解码IL-6:从免疫调控核心到临床应用的价值突破
在人体复杂的免疫调控网络中,白细胞介素6(IL-6)始终占据着核心枢纽地位。作为一种多功能细胞因子,它不仅是连接先天免疫与适应性免疫的关键桥梁,更在炎症反应、组织修复、造血调控等多个生理过程中发挥着不可替代的作用。随着生物技术的飞速发展,IL-6的作用机制被逐步解码,其在临床诊断、治疗领域的应用价值也不断凸显,成为生物医药领域的研究热点与技术转化焦点。
一、IL-6简介:免疫网络中的“多面手”
IL-6是1980年由Kishimoto团队首次发现的细胞因子,最初被命名为“B细胞刺激因子2”,因其能强效促进B细胞增殖分化并产生抗体而得名。后续研究证实,IL-6是一种分子量约26kDa的糖蛋白,主要由单核巨噬细胞、T细胞、B细胞、成纤维细胞以及内皮细胞等多种细胞在炎症刺激、微生物感染或免疫激活状态下分泌产生。
与其他细胞因子相比,IL-6的显著特点是“多功能性”——它既能调控免疫细胞的生长、分化与活化,参与免疫应答的启动与放大;也能作用于肝脏、骨髓、脂肪组织等非免疫细胞,调节急性期反应蛋白合成、造血干细胞增殖以及代谢平衡。这种广泛的作用范围,使得IL-6成为连接免疫、炎症与代谢的重要“信号中枢”,其表达水平的异常与多种疾病的发生发展密切相关。
二、
IL-6的作用方式与特点:精准调控与级联放大的双重属性
IL-6的作用方式具有鲜明的特异性与高效性,主要通过“旁分泌”“自分泌”和“内分泌”三种途径发挥作用:旁分泌途径主要作用于局部组织微环境中的邻近细胞,参与局部炎症反应与组织修复;自分泌途径则是细胞分泌的IL-6作用于自身,形成自我激活的正反馈循环;内分泌途径则是IL-6进入血液循环,作用于远端器官(如肝脏、骨髓),调控全身层面的生理过程。
其核心特点体现在“精准识别”与“级联放大”的双重属性上:一方面,IL-6必须与靶细胞表面的特异性受体(IL-6R)结合,才能启动下游信号传导,而IL-6R仅表达于肝细胞、免疫细胞等特定细胞表面,确保了作用的靶向性;另一方面,IL-6与IL-6R结合后,会进一步招募gp130分子形成异源二聚体复合物,触发下游信号通路的激活,通过级联反应实现信号的高效放大,少量IL-6即可引发显著的生物学效应。此外,IL-6的作用还具有“双向性”:生理浓度下,它参与机体正常的免疫调控与组织修复;而在病理状态下,过量表达的IL-6则会引发慢性炎症、免疫紊乱,推动疾病进展。
三、
IL-6参与的信号通路及其机制:核心通路介导的调控网络
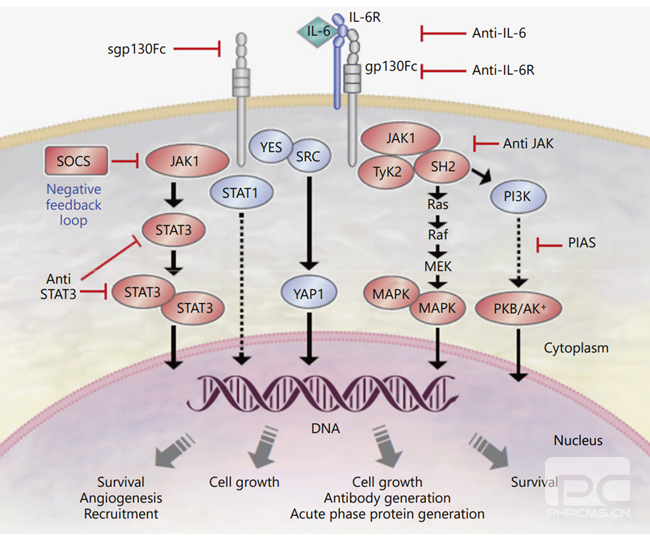
IL-6的生物学功能主要通过三条核心信号通路实现,分别是JAK-STAT通路、Ras-MAPK通路和PI3K-Akt通路,其中JAK-STAT通路是其最主要的信号传导途径。
1. JAK-STAT通路:当IL-6与靶细胞表面的IL-6R结合后,会诱导IL-6R与gp130发生聚合,进而激活与gp130胞内段结合的Janus激酶(JAK)。激活的JAK会磷酸化gp130的胞内酪氨酸残基,形成STAT蛋白的结合位点。STAT蛋白(主要是STAT3)与磷酸化的gp130结合后,会被JAK磷酸化并激活,激活后的STAT蛋白形成同源二聚体,进入细胞核内结合到下游靶基因(如急性期反应蛋白基因、抗凋亡基因等)的启动子区域,调控基因转录,从而实现对免疫细胞活化、炎症反应、细胞增殖与存活的调控。
2. Ras-MAPK通路:IL-6与受体结合激活JAK后,还可通过磷酸化Shc蛋白,启动Ras-MAPK信号通路。Shc蛋白被磷酸化后,会与Grb2、SOS形成复合物,激活Ras蛋白。激活的Ras进一步激活MAPK激酶(MEK),MEK再磷酸化激活丝裂原活化蛋白激酶(MAPK,如ERK1/2)。磷酸化的MAPK进入细胞核,调控c-Fos、c-Jun等转录因子的表达,参与细胞增殖、分化的调控,尤其在T细胞、B细胞的活化与成熟过程中发挥重要作用。
3. PI3K-Akt通路:JAK的激活还能触发PI3K-Akt通路的启动。激活的JAK可磷酸化胰岛素受体底物(IRS),促使其与PI3K结合并激活PI3K。PI3K催化磷脂酰肌醇-4,5-二磷酸(PIP2)转化为磷脂酰肌醇-3,4,5-三磷酸(PIP3),PIP3招募Akt到细胞膜并使其被PDK1磷酸化激活。激活的Akt通过磷酸化下游靶蛋白(如Bad、mTOR等),调控细胞的存活、代谢与增殖,同时还能增强STAT3的激活,进一步放大IL-6的信号效应。
三、
IL-6的临床应用:从诊断标志物到靶向治疗的全链条价值
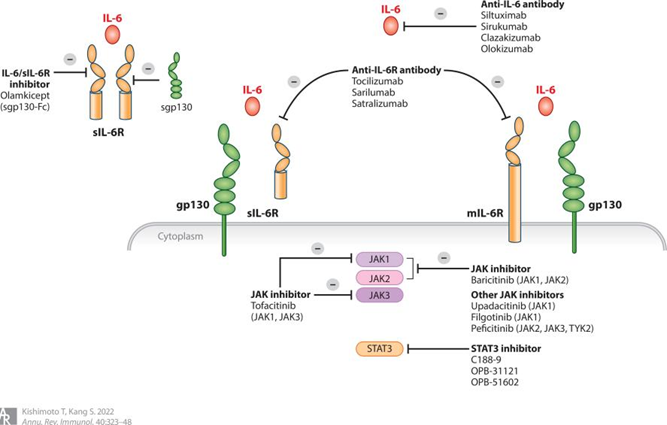
基于IL-6在疾病发生发展中的核心作用,其临床应用已覆盖疾病诊断、病情监测、靶向治疗等多个领域,成为生物医药领域的重要转化方向。
1. 疾病诊断与病情监测标志物:IL-6作为一种重要的炎症标志物,其血清水平的变化与多种疾病的发生、发展密切相关,可作为疾病诊断、病情评估与预后判断的重要指标。在脓毒症中,IL-6是早期诊断的关键标志物——脓毒症患者发病后IL-6水平会迅速升高,且升高幅度与病情严重程度正相关,比传统的CRP、降钙素原(PCT)更早出现变化,能为脓毒症的早期干预提供依据。此外,在类风湿关节炎、系统性红斑狼疮等自身免疫性疾病中,IL-6水平会持续升高,可用于疾病活动度的监测;在肿瘤领域,IL-6的高表达与肺癌、乳腺癌、多发性骨髓瘤等肿瘤的进展、转移及预后不良相关,可作为肿瘤预后评估的辅助指标。
1. 靶向IL-6的治疗药物:针对IL-6及其受体的靶向治疗是近年来的研究热点,多款药物已获批上市并应用于临床。其中,最具代表性的是抗IL-6R单克隆抗体(如托珠单抗)和抗IL-6单克隆抗体(如司妥昔单抗)。托珠单抗通过特异性结合IL-6R,阻止IL-6与受体结合,从而阻断下游信号通路的激活,已获批用于治疗类风湿关节炎、全身型幼年特发性关节炎、脓毒症等疾病,能显著改善患者的炎症症状与预后。司妥昔单抗则直接结合IL-6,抑制其生物学活性,获批用于治疗Castleman病等与IL-6过量表达相关的疾病。此外,针对JAK-STAT通路的小分子抑制剂(如托法替布),也可通过抑制IL-6信号传导,用于自身免疫性疾病的治疗,为临床治疗提供了更多选择。
2. 其他临床应用探索:除了诊断与治疗,IL-6在再生医学、疫苗研发等领域也展现出潜在应用价值。在组织修复领域,IL-6可促进成纤维细胞增殖与胶原蛋白合成,加速伤口愈合,相关研究已进入临床前阶段;在疫苗研发中,IL-6可作为免疫佐剂,增强疫苗诱导的免疫应答,提升疫苗的保护效果,目前已在多种疫苗的研发中开展探索。
结语:作为免疫调控网络中的核心分子,IL-6的作用机制与临床价值正被不断深入挖掘。从疾病诊断的精准标志物到靶向治疗的关键靶点,IL-6已成为连接基础研究与临床应用的重要桥梁。随着生物技术的持续进步,相信未来围绕IL-6的技术转化将不断突破,为炎症性疾病、自身免疫性疾病、肿瘤等多种疾病的治疗带来新的突破,守护人类健康。

