解码HMGB1:从分子机制到疾病干预的关键“信号分子”
在生物医学研究的微观世界中,一类被称为“损伤相关分子模式”(DAMPs)的蛋白质家族,正逐渐成为连接基础研究与临床转化的桥梁。其中,高迁移率族蛋白B1(High Mobility Group Box 1,HMGB1)以其复杂的功能活性、广泛的信号调控网络及在多种疾病中的核心作用,成为近年来生命科学领域的研究热点。从细胞核内的“基因守护者”到细胞外的“危险信号放大器”,HMGB1的多重身份,为疾病机制解析与新型治疗策略开发提供了重要靶点。
功能活性:从核内稳态到胞外信号的“双重角色”
HMGB1的功能活性具有显著的“位置依赖性”,其在细胞内与细胞外的生物学效应截然不同,这种特性使其成为调控细胞生理与病理过程的关键开关。
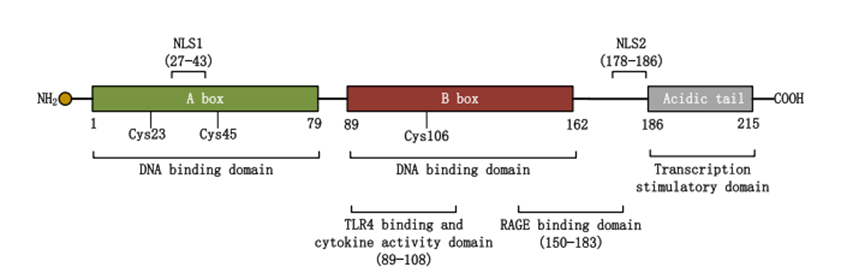
在生理状态下,HMGB1主要定位于细胞核内,作为一种非组蛋白染色体结合蛋白,它通过与DNA的小沟区域结合,参与染色质结构的维持、DNA复制、转录调控及损伤修复等核心生理过程。研究表明,HMGB1能够通过弯曲DNA链,促进转录因子与靶基因启动子区域的结合,从而调控细胞增殖、分化等关键生命活动,是维持细胞内环境稳态的重要“分子伴侣”。
当细胞受到感染、损伤或应激刺激时,HMGB1会通过主动分泌或被动释放的方式进入细胞外环境,此时其功能迅速切换为“危险信号分子”。进入胞外的HMGB1会通过其特有的结构域与免疫细胞表面的受体结合,激活免疫应答与炎症反应,启动机体的损伤修复机制。值得注意的是,胞外HMGB1的活性还受到翻译后修饰的严格调控,乙酰化、磷酸化及甲基化等修饰方式可影响其核输出效率与受体结合能力,进一步丰富了其功能调控的复杂性。
 信号通路:串联免疫与炎症的“核心调控网络”
信号通路:串联免疫与炎症的“核心调控网络”
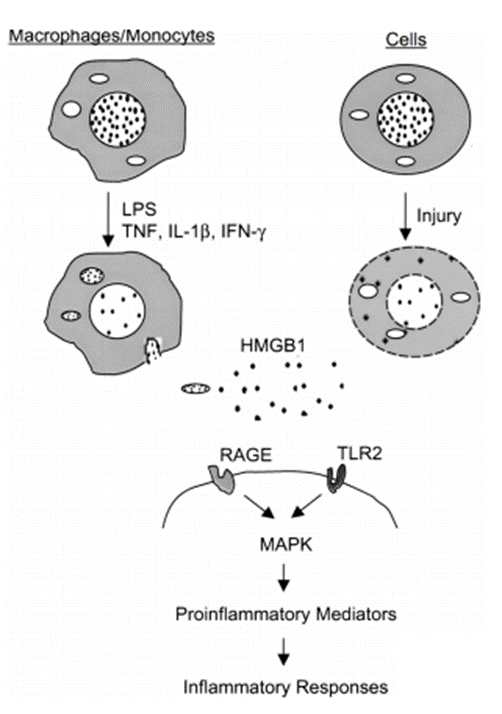
HMGB1的胞外生物学效应主要通过激活多条信号通路实现,这些通路相互交织形成复杂的调控网络,共同参与免疫应答、炎症反应及组织损伤等病理生理过程。其中,与晚期糖基化终末产物受体(RAGE)和 Toll 样受体(TLRs)的结合,是HMGB1启动信号传导的核心机制。
HMGB1与RAGE的结合可激活下游的丝裂原活化蛋白激酶(MAPK)和核因子-κB(NF-κB)信号通路。MAPK通路的激活能够促进炎症因子的转录与释放,而NF-κB作为经典的炎症调控因子,可进一步放大炎症信号,招募免疫细胞向损伤部位聚集,加速炎症反应的进程。在肿瘤微环境中,这一通路的持续激活还会促进肿瘤血管生成与肿瘤细胞的侵袭转移。
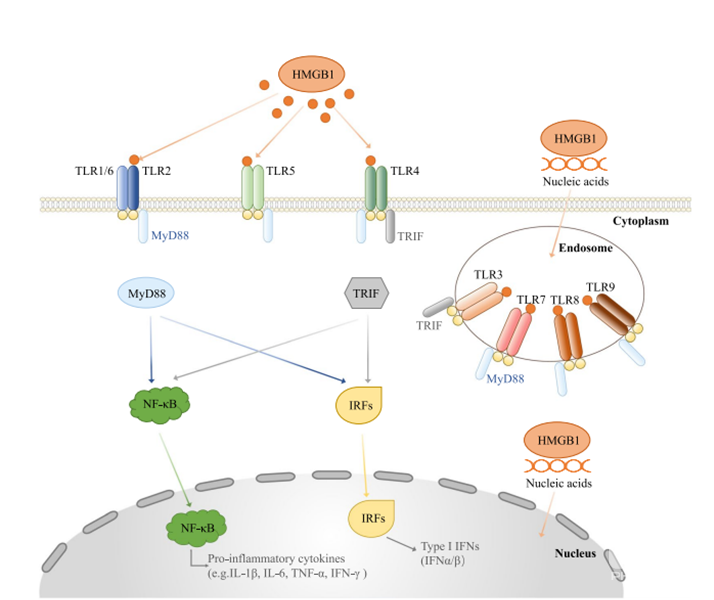
此外,HMGB1还可与TLR2、TLR4等受体结合,通过MyD88依赖型信号通路激活 innate 免疫反应。这一过程不仅在感染性疾病中发挥重要的抗感染作用,在自身免疫性疾病中也会导致免疫耐受的打破,引发自身组织的损伤。研究发现,针对HMGB1信号通路的干预,如使用RAGE拮抗剂或TLR抑制剂,能够有效抑制炎症反应的过度激活,为相关疾病的治疗提供了新的思路。
 疾病作用:从炎症到肿瘤的“多面调控因子”
疾病作用:从炎症到肿瘤的“多面调控因子”
基于其复杂的功能活性与信号调控网络,HMGB1在多种疾病的发生发展中扮演着关键角色,涉及炎症性疾病、肿瘤、神经系统疾病等多个领域,成为临床研究中极具潜力的诊断标志物与治疗靶点。
在急性炎症与感染性疾病中,HMGB1的释放水平与疾病的严重程度密切相关。在脓毒症患者体内,HMGB1作为晚期炎症因子,其血清浓度的升高往往提示预后不良。动物实验表明,中和HMGB1的活性能够显著降低脓毒症模型小鼠的死亡率,为脓毒症的治疗提供了新的方向。在类风湿关节炎等慢性炎症性疾病中,HMGB1通过持续激活炎症信号通路,促进滑膜细胞增生与炎症因子释放,加重关节组织的破坏,针对HMGB1的靶向治疗已在临床前研究中展现出良好的抗炎效果。
在肿瘤领域,HMGB1的作用呈现出“双重性”。一方面,在肿瘤发生早期,HMGB1的释放能够激活抗肿瘤免疫反应,抑制肿瘤的生长;另一方面,随着肿瘤的进展,肿瘤细胞会主动分泌HMGB1,通过激活RAGE-NF-κB通路促进肿瘤血管生成、免疫抑制微环境的形成,以及肿瘤细胞的上皮-间质转化(EMT),加速肿瘤的侵袭与转移。目前,检测肿瘤组织或血清中HMGB1的表达水平,已被用于部分肿瘤的预后评估,而HMGB1抑制剂与免疫治疗的联合应用,也成为肿瘤治疗领域的研究热点。
在神经系统疾病中,HMGB1的异常释放与缺血性脑卒中、阿尔茨海默病等疾病的病理进程密切相关。在缺血性脑卒中发生后,受损神经细胞释放的HMGB1会激活炎症反应,加重脑组织的缺血再灌注损伤;而在阿尔茨海默病患者的脑组织中,HMGB1与β淀粉样蛋白的相互作用会促进老年斑的形成,加速神经退行性病变的进展。
结语:靶向HMGB1,开启疾病治疗的新维度
从细胞核内的基础生理功能到细胞外的病理信号调控,HMGB1的多重角色使其成为生物医学研究中不可或缺的重要分子。随着对其功能活性、信号通路及疾病作用机制研究的不断深入,HMGB1在疾病诊断与治疗中的价值正逐渐凸显。无论是作为疾病进展的“风向标”,还是作为靶向治疗的“突破口”,HMGB1都为临床转化研究提供了广阔的空间。相信在未来的研究中,随着对HMGB1调控机制的进一步解码,以HMGB1为核心的新型诊断技术与治疗方案将不断涌现,为更多疾病患者带来新的希望。


