CXCL16:横跨免疫与疾病的“信号枢纽”,解锁精准诊疗新密
在人体复杂的分子信号网络中,趋化因子家族扮演着“免疫导航员”的关键角色,调控着免疫细胞的迁移、活化与组织浸润。其中,CXCL16(C-X-C基序趋化因子配体16)作为一种兼具趋化活性与受体功能的特殊分子,近年来凭借其在炎症反应、代谢调控及疾病进展中的多重作用,成为生命科学与临床诊疗领域的研究热点。从基础机制到临床转化,CXCL16正逐渐揭开神秘面纱,为多种疑难疾病的精准防控提供全新靶点与检测标尺。
一、深度解析:CXCL16的核心基本信息
CXCL16又称SR-PSOX,是人类基因组中定位为17p13.2染色体上的蛋白编码基因(Gene ID: 58191),其编码的前体蛋白含273个氨基酸,经加工后形成具有多种功能域的成熟分子。作为趋化因子超家族中仅有的两种跨膜趋化因子之一,CXCL16具有独特的分子结构:胞外区域包含CXC趋化因子结构域和粘蛋白样间隔区,胞内区域则带有潜在的酪氨酸磷酸化位点,这种结构使其既能锚定在细胞表面,也可通过ADAM10等蛋白酶剪切形成可溶性分子发挥作用。
在组织分布上,CXCL16具有广泛的表达特性,其中肺(RPKM 40.7)、睾丸(RPKM 23.8)及多种免疫相关组织中表达水平较高,而在大脑、骨髓、骨骼肌等组织中则几乎不表达。细胞层面,CXCL16主要分布于CD19⁺ B细胞、CD14⁺单核/巨噬细胞及树突状细胞表面,这些细胞也正是其发挥免疫调控功能的核心载体。
二、多元调控:CXCL16的复杂作用机制
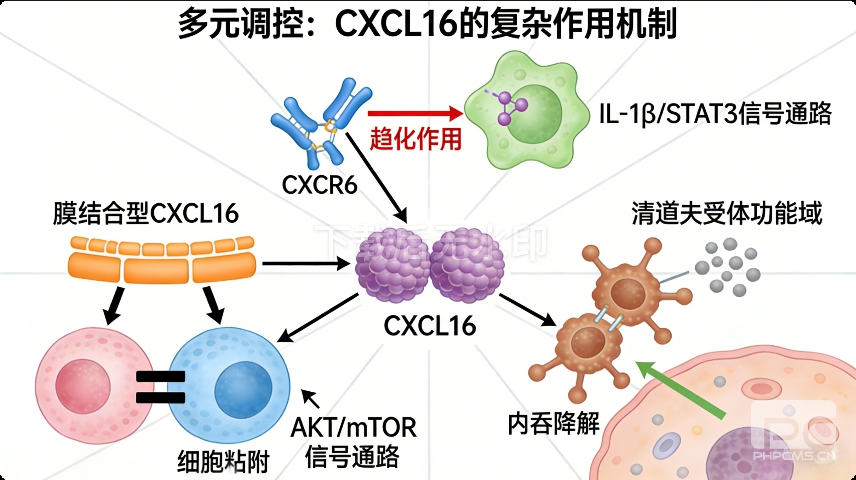
CXCL16的功能实现主要依赖于其与唯一受体CXCR6的特异性结合,同时兼具趋化因子、粘附分子和清道夫受体三重生物学活性,形成了多维度的调控网络。
首先,作为趋化因子,可溶性CXCL16可精准招募表达CXCR6的T细胞、自然杀伤细胞(NK细胞)及NKT细胞向炎症部位或损伤组织迁移,启动局部免疫应答。例如在银屑病发病机制中,CXCL16通过与CXCR6结合,招募CXCR6⁺Vγ2⁺γδT17细胞或CD8⁺Tc17细胞聚集于表皮,分泌IL-17A引发持续炎症反应。其次,膜结合型CXCL16可作为粘附分子,介导免疫细胞与内皮细胞、实质细胞的粘附,促进免疫细胞的组织浸润与活化。最后,CXCL16还具备清道夫受体功能,能够结合并摄取细菌、氧化脂蛋白等物质,参与机体的抗感染免疫与脂质代谢调控,其介导的泡沫细胞形成过程更是动脉粥样硬化发生发展的关键环节之一。
此外,CXCL16的表达调控还涉及多条信号通路的协同作用。如在银屑病中,UBE2L3缺失可通过IL-1β/STAT3信号通路促进CXCL16上调,形成正反馈环路驱动炎症进展;而在脓毒症中,miR-625-5p可通过调控CXCL16/CXCR6轴影响内皮屏障功能,这为相关疾病的靶向干预提供了新的机制依据。
 三、疾病关联:CXCL16成为多系统疾病的“关键节点”
三、疾病关联:CXCL16成为多系统疾病的“关键节点”
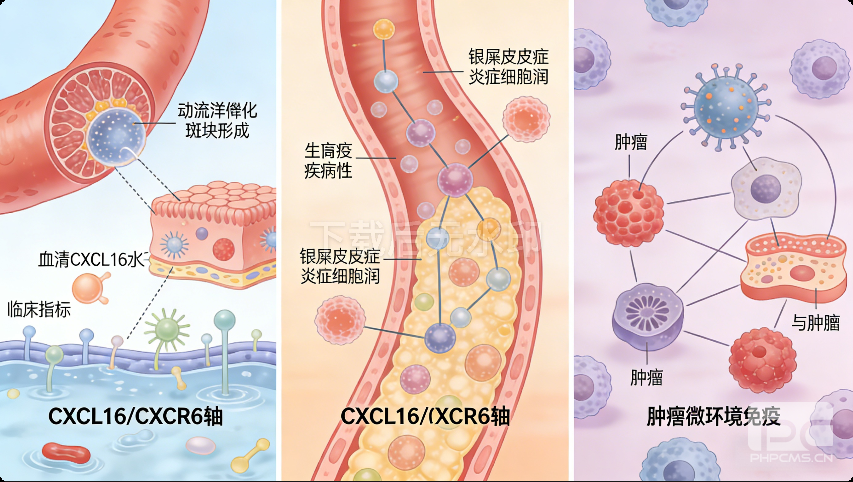
随着研究的深入,CXCL16已被证实与多种炎症性疾病、代谢性疾病、肿瘤及感染性疾病密切相关,其表达水平的异常改变往往预示着疾病的发生、进展与预后。
在心血管疾病领域,CXCL16是动脉粥样硬化的重要调控因子。研究发现,CXCL16基因多态性与冠状动脉狭窄严重程度相关,其血清水平升高还与动脉粥样硬化性卒中风险增加密切相关。膜结合型CXCL16通过介导T细胞粘附与脂质摄取促进斑块形成,而可溶性CXCL16则驱动炎症细胞迁移加剧斑块不稳定性,这使其成为心血管疾病风险评估的潜在生物标志物。
在自身免疫性疾病中,CXCL16/CXCR6轴的异常激活尤为关键。浙江大学满孝勇教授团队的研究证实,CXCL16在银屑病表皮中高表达,阻断CXCL16可显著减轻银屑病样皮损,为临床治疗提供了新靶点。此外,CXCL16还与系统性硬化症、多发性硬化症等疾病相关,其基因多态性可影响疾病易感性与病情严重程度。
在肿瘤领域,CXCL16呈现出“双面性”:膜结合型CXCL16可促进肿瘤周围淋巴细胞聚集,与肿瘤患者良好预后相关;而可溶性CXCL16则通过激活AKT/mTOR信号通路增强肿瘤细胞的增殖与迁移能力,促进肿瘤进展。在三阴性乳腺癌中,ELK3-CXCL16轴可通过调控NK细胞细胞毒性影响肿瘤免疫监视,这为肿瘤免疫治疗提供了新的切入点。
除此之外,CXCL16还与COVID-19、慢性阻塞性肺疾病(COPD)、肥胖、椎间盘退变等疾病存在关联。如在COPD患者中,肺泡巨噬细胞中CXCL16表达下调可通过破坏免疫代谢稳态驱动疾病进展;而COVID-19住院患者中,CXCL16水平与疾病不良结局及心脏受累密切相关,使其成为相关疾病诊断与预后评估的潜在指标。
 四、检测技术:精准捕获CXCL16,助力临床转化应用
四、检测技术:精准捕获CXCL16,助力临床转化应用
CXCL16在疾病诊断、预后评估及疗效监测中的应用,离不开精准、高效的检测技术。目前,针对CXCL16的检测方法已日趋成熟,涵盖酶联免疫吸附试验(ELISA)、Western Blot、流式细胞术、免疫组织化学等多种技术平台,其中ELISA因操作简便、灵敏度高、特异性强等优势,成为临床样本检测的主流方法。
市面上已出现多款针对人、小鼠等物种的CXCL16 ELISA试剂盒,可实现对血清、血浆、组织标本等多种样本中CXCL16的定量检测。以DLdevelop的人CXCL16 ELISA试剂盒(
DLR-CXCL16-Hu)为例,灵敏度高达0.067ng/mL,检测范围覆盖0.156-10ng/mL,且具备良好的抗干扰性,检测时间仅需3.5小时,显著优于常规ELISA试剂盒。
此外,荧光标记抗体技术的应用进一步提升了CXCL16检测的精准度与可视化效果。这些检测技术的发展,不仅为CXCL16的基础研究提供了支撑,更推动了其在临床诊疗中的转化应用,使CXCL16成为精准医疗的重要“抓手”。
五、总结与展望:CXCL16的临床转化潜力可期
作为兼具多重生物学功能的分子“信号枢纽”,CXCL16在免疫调控、代谢平衡与疾病进展中发挥着不可替代的作用。其与多系统疾病的密切关联,使其成为疾病诊断的潜在生物标志物、预后评估的重要指标及靶向治疗的核心靶点。随着检测技术的不断革新与基础研究的持续深入,CXCL16的临床转化价值将得到进一步释放,有望在心血管疾病、自身免疫性疾病、肿瘤等多种疾病的精准防控中发挥关键作用。
未来,随着CXCL16调控机制的进一步阐明,以及靶向药物与检测试剂的迭代升级,我们有理由相信,这一“多面手”分子将为人类健康事业带来更多突破,开启精准诊疗的全新篇章。

