解码免疫“信号兵”IFN-γ:从分子机制到临床应用的全景洞
在人体复杂的免疫防御网络中,有一种细胞因子被誉为“免疫信号的关键传递者”,它既能唤醒沉睡的免疫细胞,又能精准狙击病原体与异常细胞,它就是γ-干扰素(Interferon-γ,IFN-γ)。从基础免疫学研究到肿瘤、感染性疾病等临床诊疗领域,IFN-γ的每一个分子机制都承载着突破医学瓶颈的可能,每一次检测技术的升级都为疾病诊断提供了更精准的依据。
一、IFN-γ:免疫网络中的“多功能信号中枢”
IFN-γ是II型干扰素家族的核心成员,1973年首次被科学家发现并命名。与I型干扰素(如IFN-α/β)主要参与抗病毒先天免疫不同,IFN-γ是一种典型的“后天免疫调节因子”,主要由活化的T淋巴细胞(如Th1细胞、细胞毒性T细胞)和自然杀伤细胞(NK细胞)分泌产生。其分子结构为同源二聚体,通过与靶细胞表面的特异性受体(IFN-γR)结合发挥作用,这种高度特异性的结合模式,确保了免疫信号传递的精准性,避免了免疫反应的紊乱。
作为免疫网络的“中枢节点”,IFN-γ的特殊性在于它既能连接先天免疫与适应性免疫,又能调控免疫细胞的分化与功能,这种“承上启下”的特性,使其成为免疫研究领域的“明星分子”。
二、信号通路:精密调控的“分子传导链”
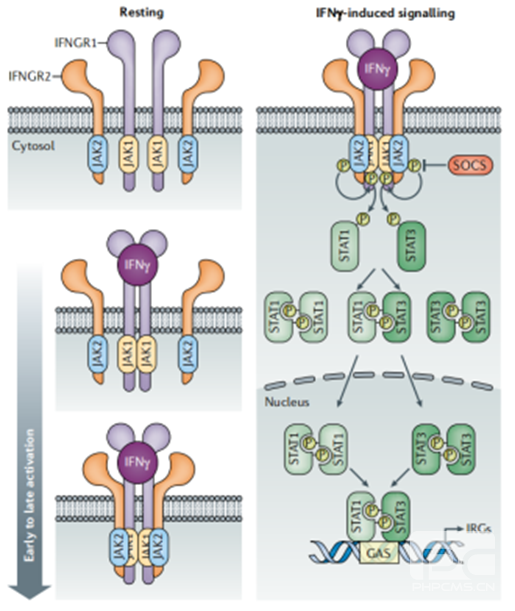
IFN-γ的生物功能依赖于一套高度保守且精密的信号传导通路——JAK-STAT通路,其传导过程如同一条“精准高效的分子电路”,每一步都经过严格调控,确保信号不被干扰或误传。
当IFN-γ二聚体与靶细胞膜上的IFN-γR1/IFN-γR2异二聚体受体结合后,首先激活受体胞内结构域偶联的JAK激酶(JAK1和JAK2),激活后的JAK激酶发生自身磷酸化并进一步磷酸化受体的酪氨酸残基,形成“信号锚定位点”。随后,胞质中的STAT1分子被招募到受体磷酸化位点,通过JAK激酶的作用发生酪氨酸磷酸化,磷酸化的STAT1分子迅速形成同源二聚体(即GAF复合物)。
形成的GAF复合物具备核定位能力,能够穿过核膜进入细胞核内,与靶基因启动子区域的“γ-干扰素激活序列(GAS)”特异性结合,从而启动一系列下游基因的转录表达,这些基因包括调控免疫细胞活化的细胞因子基因、抑制病原体复制的抗病毒基因以及参与细胞凋亡调控的肿瘤抑制基因等。值得注意的是,这条通路中还存在负调控因子(如SOCS家族蛋白),能够及时终止信号传导,避免免疫反应过度激活对正常细胞造成损伤,体现了生物调控的“平衡智慧”。
三、核心功能:免疫防御与细胞调控的“多面手”
IFN-γ的功能覆盖免疫防御、细胞稳态调控等多个维度,其作用机制的多样性使其在生物医学领域具有广泛的应用潜力。
在免疫防御方面,IFN-γ是对抗胞内病原体(如结核分枝杆菌、乙肝病毒、HIV等)的“核心武器”。它能够激活巨噬细胞的吞噬杀伤功能,促进巨噬细胞产生活性氧(ROS)和一氧化氮(NO),增强对胞内寄生菌和病毒的清除能力;同时,IFN-γ还能促进树突状细胞的成熟,增强其抗原提呈能力,从而激活更多特异性T淋巴细胞参与免疫反应,形成“持续免疫记忆”。
在肿瘤免疫调控中,IFN-γ发挥着“双重作用”:一方面,它能够直接抑制肿瘤细胞的增殖,诱导肿瘤细胞发生凋亡,同时通过上调肿瘤细胞表面MHC-I类分子的表达,增强肿瘤细胞的“免疫原性”,使肿瘤细胞更容易被细胞毒性T细胞识别和杀伤;另一方面,IFN-γ还能调控肿瘤微环境,抑制免疫抑制性细胞(如Treg细胞、M2型巨噬细胞)的活性,打破肿瘤的“免疫逃逸”屏障,为肿瘤免疫治疗提供“有利环境”。
此外,IFN-γ在免疫耐受调控、炎症反应平衡等方面也发挥着重要作用。它能够调节Th1/Th2细胞亚群的分化平衡,避免因Th2细胞过度激活导致的过敏性疾病;同时,在自身免疫性疾病中,IFN-γ的表达异常也与疾病的发生发展密切相关,体现了其“双刃剑”特性。
四、疾病关联:临床诊断与治疗的“关键生物标志物”
IFN-γ的表达水平与多种疾病的发生发展、病情严重程度及预后密切相关,使其成为临床诊疗中极具价值的“生物标志物”和治疗靶点。
在感染性疾病领域,IFN-γ的检测是结核分枝杆菌感染诊断的“金标准”之一。由于结核分枝杆菌感染后,机体的特异性T细胞会在抗原刺激下分泌IFN-γ,通过检测外周血中特异性T细胞分泌IFN-γ的水平(如T-SPOT.TB检测),能够快速、准确地诊断潜伏性结核感染,避免了传统痰培养方法耗时久、敏感性低的缺陷。在病毒性肝炎(如乙肝、丙肝)中,IFN-γ的表达水平与肝脏炎症程度正相关,高表达的IFN-γ提示机体抗病毒免疫反应活跃,可为临床治疗方案的选择提供参考。
在肿瘤领域,IFN-γ的表达模式与肿瘤预后密切相关。研究表明,肿瘤微环境中IFN-γ水平较高的患者,接受免疫检查点抑制剂(如PD-1/PD-L1抑制剂)治疗的疗效更好,因为IFN-γ能够增强肿瘤微环境的免疫活性,提高免疫治疗的响应率。此外,IFN-γ信号通路的异常激活或抑制也与肿瘤的发生密切相关,例如STAT1基因突变导致IFN-γ信号通路缺陷,会增加肿瘤的发生风险。
在自身免疫性疾病中,IFN-γ的异常高表达是重要的致病因素之一。在类风湿关节炎、系统性红斑狼疮等疾病中,免疫细胞过度分泌IFN-γ,导致炎症反应加剧,组织器官损伤。因此,靶向IFN-γ信号通路的药物(如抗IFN-γ单克隆抗体)已成为自身免疫性疾病治疗的新方向。
五、检测技术:从基础研究到临床应用的“精准工具”
随着生物技术的发展,IFN-γ的检测技术不断升级,从早期的生物活性测定到如今的分子水平检测,检测的敏感性、特异性和时效性均得到了显著提升,为基础研究和临床诊疗提供了有力支撑。
传统的检测方法以生物活性测定法为主,通过检测IFN-γ对敏感细胞系(如L929细胞)的抗病毒活性或增殖抑制作用来间接定量IFN-γ的水平,该方法能够反映IFN-γ的生物功能,但操作复杂、耗时久,且易受其他细胞因子的干扰,逐渐被更精准的方法取代。
酶联免疫吸附试验(ELISA)是目前临床应用最广泛的IFN-γ检测方法,基于抗原-抗体特异性结合的原理,通过酶标记抗体实现对IFN-γ的定量检测。该方法操作简便、特异性高,能够快速检测血清、血浆等样本中的IFN-γ水平,广泛应用于感染性疾病的辅助诊断和疗效监测。
针对细胞水平IFN-γ的检测,酶联免疫斑点试验(ELISPOT)和流式细胞术(FCM)成为主流技术。ELISPOT能够检测单个细胞分泌IFN-γ的能力,敏感性极高,可用于结核感染的特异性诊断、肿瘤特异性T细胞的筛选等;流式细胞术则通过荧光标记抗体检测细胞内IFN-γ的表达,能够同时分析不同细胞亚群(如Th1细胞、NK细胞)分泌IFN-γ的情况,为免疫功能评估提供更细致的信息。
在分子水平,实时荧光定量PCR(qPCR)技术可通过检测IFN-γ基因的mRNA表达水平,反映IFN-γ的转录活性,用于疾病早期诊断、发病机制研究等领域。此外,基于微流控芯片、电化学传感器等新型检测技术的研发,进一步实现了IFN-γ的快速、微量检测,为床旁诊断(POCT)提供了可能。
结语:IFN-γ——连接基础研究与临床应用的“桥梁分子”
从免疫信号的精准传递到疾病的临床诊疗,IFN-γ的每一个分子特性都彰显着生物医学的魅力。随着对其信号通路机制的深入解析、检测技术的不断创新以及靶向药物的研发突破,IFN-γ在感染性疾病、肿瘤、自身免疫性疾病等领域的应用前景将更加广阔。未来,随着多组学技术、基因编辑技术与IFN-γ研究的深度融合,我们将进一步揭开其分子机制的神秘面纱,让这一免疫“信号兵”在守护人类健康的道路上发挥更大的作用。

